Le marché de l’immuno-oncologie (IO) connaît une croissance robuste, le marché mondial des médicaments d’IO, y compris les inhibiteurs de points de contrôle, devant atteindre plus de 109 milliards de dollars en 2025 et dépasser les 400 milliards de dollars d’ici 2034. Cette forte augmentation est due à l’augmentation de l’incidence mondiale du cancer, aux investissements importants dans la R&D et à l’élargissement des indications des immunothérapies. Les inhibiteurs de points de contrôle, en particulier ceux qui ciblent PD-1/PD-L1 et CTLA-4, dominent le marché et génèrent la majorité des revenus des médicaments d’IO grâce à leur large autorisation dans le traitement des tumeurs solides et hématologiques malignes. Cependant, malgré des progrès spectaculaires, une proportion importante de patients atteints de cancer ne parvient toujours pas à obtenir de réponses durables, principalement parce que de nombreuses tumeurs maintiennent un microenvironnement immunosuppresseur ou « froid » qui réduit l’efficacité des thérapies existantes.
Situation actuelle et besoins non satisfaits
- Thérapies actuelles : Les principaux inhibiteurs de points de contrôle utilisés en clinique comprennent les inhibiteurs de CTLA-4 (par exemple, l’ipilimumab), les inhibiteurs de PD-1 (par exemple, le pembrolizumab, le nivolumab) et les inhibiteurs de PD-L1 (par exemple, l’atezolizumab, le durvalumab), approuvés pour divers cancers tels que le mélanome, le cancer du poumon, du rein, de la vessie….
- Besoins des patients :
- Les besoins non satisfaits persistants comprennent l’augmentation des taux de rémission durable,
- le dépassement de la résistance primaire et secondaire,
- la réduction des effets indésirables liés au système immunitaire,
- Une offre d’options efficaces pour les patients atteints de tumeurs « froides » ou pauvre en composant du système immunitaire.
Lacunes thérapeutiques : jusqu’à 70 % des patients peuvent ne pas bénéficier à long terme du blocage des inhibiteurs de points de contrôle et nécessiter des agents d’IO novateurs, combinatoires ou de nouvelle génération.
OPM-101 en résumé
- Classe de composés : petite molécule inhibitrice de RIPK2, hautement sélective et administrable par voie orale
- Mécanisme : inhibition sélective de la voie NOD2/RIPK2.
OPM-101 est conçu pour reprogrammer les réponses immunitaires dans le cancer, surmonter les principaux mécanismes de résistance et libérer tout le potentiel de l’immunothérapie. - Indication : patients atteints d’un cancer résistant aux inhibiteurs de points de contrôle immunitaires
- Phase clinique : phase 1 terminée (SAD & MAD) ; phase 1b/2a chez les patients atteints d’un mélanome présentant une résistance secondaire aux inhibiteurs de points de contrôle en cours de planification ; association avec un anti-PD1
- Profil pharmacocinétique : absorption rapide, demi-vie longue
- Sécurité : excellente ; aucun événement indésirable grave
- Engagement de la cible : inhibition robuste et soutenue du TNF-α, même à faibles doses
- Différenciateur clé : s’attaque à la fois aux mécanismes de résistance dans le microenvironnement tumoral et à la présentation des néoantigènes sur les cellules cancéreuses
Application potentielle
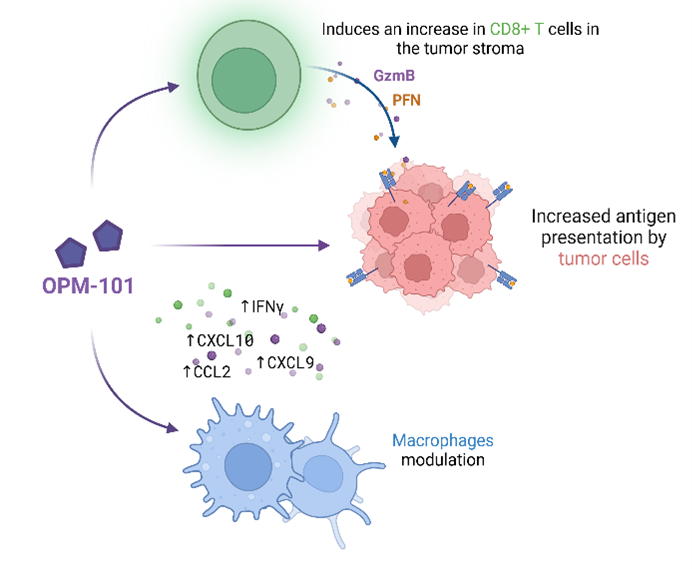
RIPK2 est un régulateur central de la signalisation immunitaire dans le microenvironnement tumoral, influençant le comportement des cellules immunitaires innées et adaptatives. Des recherches récentes démontrent qu’une expression élevée de RIPK2 dans les tumeurs contribue à la résistance à l’immunothérapie, notamment en altérant les réponses des lymphocytes T cytotoxiques et en favorisant un milieu tumoral suppressif. En inhibant RIPK2, il est possible de reprogrammer le microenvironnement tumoral, de restaurer l’activité des lymphocytes T et de sensibiliser les tumeurs auparavant non réceptives à l’inhibition des points de contrôle. De plus, il a été démontré que l’inhibition de RIPK2 exerce un effet direct sur les cellules cancéreuses en augmentant la présentation des antigènes.
En résumé, si les inhibiteurs de point de contrôle ont transformé le traitement du cancer, il existe toujours un besoin critique de modalités innovantes telles que l’inhibition de RIPK2 afin d’étendre et de maintenir les réponses chez une population de patients plus large.
Effets potentiels d’OPM-101 dans l’I/O :
1) Moduler le microenvironnement tumoral vers un état inflammatoire plus élevé
2) Augmenter la présentation des antigènes sur les cellules cancéreuses
État d’avancement du développement :
Points forts de la phase 1
- Volontaires sains : phase de doses uniques croissantes (SAD) avec des doses allant de 5 à 1 000 mg (y compris des cohortes dédiées à l’effet alimentaire et une cohorte de femmes). Phase de doses multiples croissantes (MAD) avec des doses allant de 75 à 300 mg deux fois par jour pendant 14 jours.
- Étude randomisée, contrôlée par placebo, explorant les paramètres PK/PD, la sécurité et l’engagement cible.
- Résultats : OPM-101 présente une absorption rapide et une demi-vie longue de 12 heures. La sécurité est excellente, sans événement indésirable grave, même aux doses les plus élevées. L’engagement de la cible est solide, avec une inhibition soutenue du TNF-α, même à faibles doses.
Statut de propriété intellectuelle
- Structure chimique différenciée des autres inhibiteurs de RIPK2 grâce à la technologie Nanocyclix® d’OPM.
- Brevet de composition de matière déposé en 2016, accordé dans la plupart des pays, y compris les 5MM. Invention de sélection avec OPM-101 et analogues déposée en 2021.
Possibilité de licence
OPM-101 est disponible pour l’octroi de licences à l’échelle mondiale et pour le développement régional spécifique, ainsi que pour l’acquisition potentielle d’actifs dans le monde entier.